Fórmula química é uma representação gráfica de um composto químico. Ela representa o número e o tipo de átomo que constituem uma molécula. É o modo abreviado para representar as reações químicas através de símbolos químicos.
Matéria, compostos e elementos
Tudo o que nos rodeia é matéria. Pode-se definir matéria como tudo aquilo que ocupa lugar no espaço e tem massa. A matéria é, portanto, formada por substâncias puras e misturas.
Substâncias puras podem ser elementos ou compostos. Água, ferro, oxigênio, açúcar e butano são exemplos de substâncias puras.
Por isso a substância pura tem uma composição fixa e apresenta propriedades constantes em toda sua extensão.
Há substâncias puras, porém, que podem ser decompostas em outras mais simples e são chamadas de compostos.
A água, por exemplo, é decomposta em dois gases: oxigênio e hidrogênio. Esses gases são exemplos de elementos, substâncias puras que não podem ser decompostas por nenhum procedimento.
Nesse sentido, os elementos também são chamados de substâncias simples. E os compostos de substâncias compostas, formadas por dois ou mais tipos de partículas.
Símbolos
O químico e físico inglês John Dalton (1766-1844), em princípios do século XIX, propôs uma série de símbolos para representar elementos químicos conhecidos até então.
Essa série de desenhos foram compilados à medida que se conheciam novos elementos.
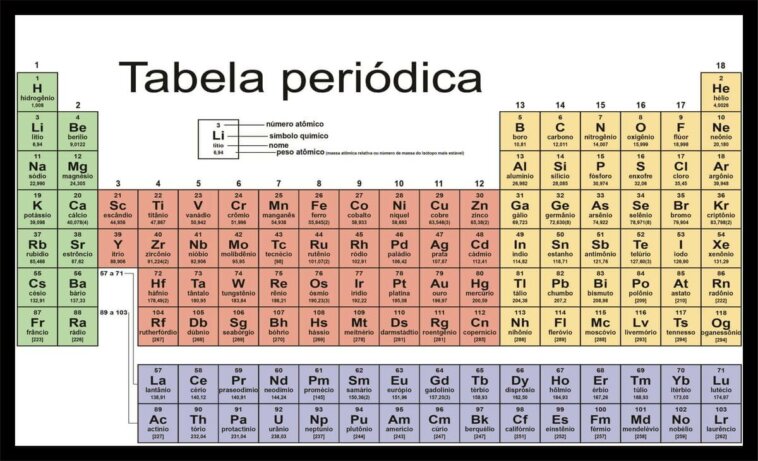
Foi o médico e químico sueco Johs Jakob Berzelius (1779-1848) quem sugeriu a simbologia usada atualmente, da tabela periódica:
– Cada elemento químico é representado por um símbolo, que pode ser a letra inicial do nome do elemento em caractere maiúsculo. Por exemplo, hidrogênio (H), oxigênio (O).
– Para evitar iniciais repetidas, alguns tem a segunda letra acompanhada também. No caso de cálcio (Ca) ou berílio (Be).
– Alguns elementos são representados pelos símbolos de seus nomes em latim, como ouro – aurum (Au), ou do grego, hélio – hélios (He).
Fórmulas
As substâncias são representadas por fórmulas. As fórmulas indicam quais são os componentes que constituem a substância, assim como as proporções em que eles se encontram.
No caso de uma molécula de ácido sulfúrico, por exemplo: H₂SO₄. Por meio de sua fórmula, podemos constatar que há dois átomos de hidrogênio, um átomo de enxofre e quatro átomos de oxigênio.
Tipos de fórmulas
Essa fórmula acima exemplificada de ácido sulfúrico é a fórmula molecular dos compostos. Como exemplificamos, ela mostra de forma simples a constituição da molécula, os átomos e suas quantidades.
Além da fórmula molecular, que é a mais comum, há também os outros tipos seguintes:
– Fórmula mínima: que é a simplificação da fórmula molecular. Muitas vezes, como é o caso do ácido sulfúrico, não há como simplificar mais. Portanto a fórmula mínima é a mesma da molecular.
– Fórmula eletrônica: uma fórmula mais complexa, pois além de mostrar os átomos e suas quantidades, também indica os elétrons da camada de valência de cada átomo e a formação dos pares eletrônicos.
– Fórmula estrutural plana ou simplificada: a fórmula estrutural de Couper é a representação mais gráfica dos compostos. Há as ligações entre os átomos, sendo cada par de elétrons entre os átomos representados por um traço.
– Fórmula porcentual: indica a porcentagem da massa de cada um dos elementos dos compostos.
H2SO4: H 2,04%, S 32,65%, O 65,31%.
Exercícios
Exemplo de exercício para calcular a massa detalhada dos compostos:
H2SO4 (H = 1, S = 32, O = 16)
MM = 98u
98u—-100% da massa de H2SO4
2u H— x
x = 2,04 % de hidrogênio
98u—– 100%
32u S—- x
x = 32,65% de enxofre
98u —– 100%
64u O— x
x = 65,31% de oxigênio
Outros tipos de exercícios comuns:
A maioria dos exercícios em vestibulares pede que você faça a relação entre as fórmulas, encontrando dados, chegando a novos resultados a partir dos dados disponibilizados. Não se preocupe, os dados serão sempre disponibilizados.
O mais importante é você aprender a ler e a escrever cada uma das fórmulas, sabendo identificar também as representações e os nomes dos elementos e, portanto, dos compostos.
Portanto, para você que irá prestar um concurso vestibular ou o Enem, fique atento e priorize o estudo de fórmulas químicas.